A partir del 12 de marzo de 2020, la enfermedad por coronavirus 2019 (COVID-19) se ha confirmado en 125.048 personas en todo el mundo, con una mortalidad de aproximadamente 3,7%, en comparación con una tasa de mortalidad de influenza inferior al 1%.
Hay una necesidad urgente de un tratamiento efectivo.
El enfoque actual ha estado en el desarrollo de nuevas terapias, que incluyen antivirales y vacunas. La evidencia acumulada sugiere que un subgrupo de pacientes con COVID-19 grave podría tener un síndrome de tormenta de citoquinas. Recomendamos la identificación y el tratamiento de la hiperinflamación utilizando terapias aprobadas existentes con perfiles de seguridad comprobados para abordar la necesidad inmediata de reducir la mortalidad en aumento.
El tratamiento actual de COVID-19 es de apoyo, y la insuficiencia respiratoria por síndrome de dificultad respiratoria aguda (SDRA) es la principal causa de mortalidad.
|
Al igual que durante las pandemias anteriores (síndrome respiratorio agudo severo y síndrome respiratorio del Medio Oriente), los corticosteroides no se recomiendan de manera rutinaria y pueden exacerbar la lesión pulmonar asociada a COVID-19.
Sin embargo, en la hiperinflamación, es probable que la inmunosupresión sea beneficiosa.
El nuevo análisis de los datos de un ensayo controlado aleatorizado de fase 3 del bloqueo de IL-1 (anakinra) en la sepsis, mostró un beneficio de supervivencia significativo en pacientes con hiperinflamación, sin mayores eventos adversos.
Se aprobó un ensayo controlado aleatorio multicéntrico de tocilizumab (bloqueo del receptor de IL-6, con licencia para el síndrome de liberación de citoquinas), en pacientes con neumonía por COVID-19 e IL-6 elevada en China (ChiCTR2000029765). La inhibición de la Janus quinasa (JAK) podría afectar tanto la inflamación como la entrada viral celular en COVID-19.
Todos los pacientes con COVID-19 grave deben someterse a pruebas de detección de hiperinflamación utilizando tendencias de laboratorio (p. Ej., aumento de ferritina, disminución del recuento de plaquetas o velocidad de sedimentación globular) y HScore (tabla) para identificar el subgrupo de pacientes para quienes la inmunosupresión podría mejorar la mortalidad.
Las opciones terapéuticas incluyen esteroides, inmunoglobulina intravenosa, bloqueo selectivo de citocinas (p. Ej., Anakinra o tocilizumab) e inhibición de JAK.
- El Hscore genera una probabilidad de la presencia de HLH secundario.
- Los puntajes HS superiores a 169 son 93% sensibles y 86% específicos para HLH.
- Tenga en cuenta que la hemofagocitosis de la médula ósea no es obligatoria para el diagnóstico de HLH.
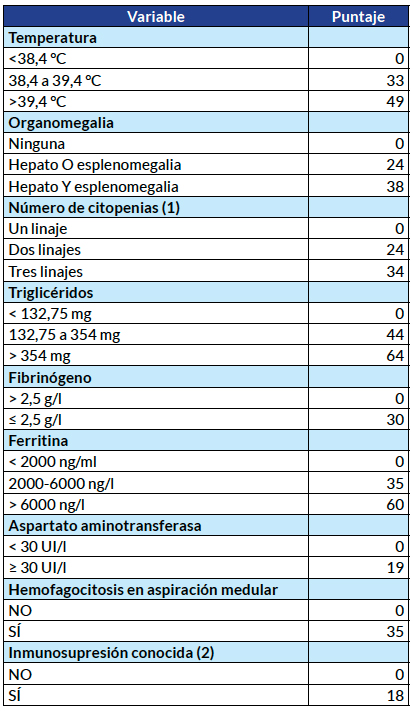
Los puntajes HS se pueden calcular usando una calculadora HScore en línea. HLH = linfohistiocitosis hemofagocítica. *(1) Definido como una concentración de hemoglobina de 9 · 2 g / dL o menos (≤5 · 71 mmol / L), un recuento de glóbulos blancos de 5000 glóbulos blancos por mm3 o menos, o un recuento de plaquetas de 110 000 plaquetas por mm3 o menos, o todos estos criterios combinados. (2) VIH positivo o que recibe terapia inmunosupresora a largo plazo (es decir, glucocorticoides, ciclosporina, azatioprina).
Declaraciones de los autores:
PM es becario de capacitación clínica dentro de la red de la Iniciativa de Medicina Experimental para Explorar Nuevas Terapias y recibe fondos del proyecto no relacionados con esta Correspondencia. PM también recibe cofinanciación del Centro de Investigación Biomédica del Hospital Universitario de Londres del Instituto Nacional de Investigación en Salud (NIHR). DFM preside el comité de financiación del Consejo de Investigación Médica y NIHR para COVID-19 para terapias y vacunas. DFM informa honorarios personales de consultoría para ARDS para GlaxoSmithKline, Boehringer Ingelheim y Bayer; Además, su institución ha recibido fondos de subvenciones del Reino Unido NIHR, Wellcome Trust, Innovate UK y otros, todos ellos no relacionados con esta correspondencia. DFM también tiene una patente emitida a su institución para un tratamiento para el SDRA. DFM es Director de Investigación de la Sociedad de Cuidados Intensivos y Director del Programa de Evaluación de Eficacia y Mecanismo de NIHR. Todos los demás autores declaran no tener intereses en competencia.